Изотопы
– разновидности одного того же элемента, отличающиеся массой ядер (массовым числом А) пpи одинаковом атомном номере (заряде
ядра). Атомные ядра И. данного элемента содержат одинаковое число протонов при различном
числе нейтронов. В ядерной астрофизике
рассматриваются npоцессы нейтронного захвата, к-рые приводят к образованию И. данного
элемента с последовательно возрастающим числом А до тех пор, пока не получится
И., неустойчивый по отношению к бета-процессам.
Последний приводит к образованию одного из изотопов следующего (по атомному номеру)
элемента. Общее число стабильных изотопов 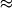 300. Общее число известных
в настоящее время изотопов, включая нестабильные,
300. Общее число известных
в настоящее время изотопов, включая нестабильные, 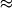 1500. Примеры:
изотопы водорода 1H, 2D (тяжёлый
водород, дейтерий), 3Т (тритий - нестабилен, период полураспада
T1/2=12,4 года); изотопы гелия 3Не,
4Не (наиболее распространённый), 6Не
(нестабилен, T1/2= 0,8 с), 8Не
(нестабилен, T1/2= 0,122 с).
1500. Примеры:
изотопы водорода 1H, 2D (тяжёлый
водород, дейтерий), 3Т (тритий - нестабилен, период полураспада
T1/2=12,4 года); изотопы гелия 3Не,
4Не (наиболее распространённый), 6Не
(нестабилен, T1/2= 0,8 с), 8Не
(нестабилен, T1/2= 0,122 с).
"Физика Космоса", 1986
Глоссарий Astronet.ru
Публикации с ключевыми словами:
изотопы
Публикации со словами:
изотопы
|

|
См. также:
|
